注意!PBMC复苏后计数,不同计数仪结果差异巨大,千万别被数据“骗”了!
在做免疫学、细胞治疗或疫苗研发的朋友们,一定对PBMC(外周血单个核细胞)不陌生。它可是我们研究T细胞、B细胞、NK细胞的重要“原材料”。
然而,有一个非常常见却又容易被忽视的问题——PBMC复苏后的细胞计数,用不同计数仪,结果竟然完全不同!
误差到底有多大?我们直接用数据说话。
实验小剧场
我们做了3组对比实验:
➡ 样本来源:同一份冻存的PBMC,相同复苏操作,分别计数3个批次样本;
➡ 计数仪类型:自动细胞计数仪A、自动细胞计数仪B、血球计数板(人工)
结果如下(单位:10⁶ cells/mL)
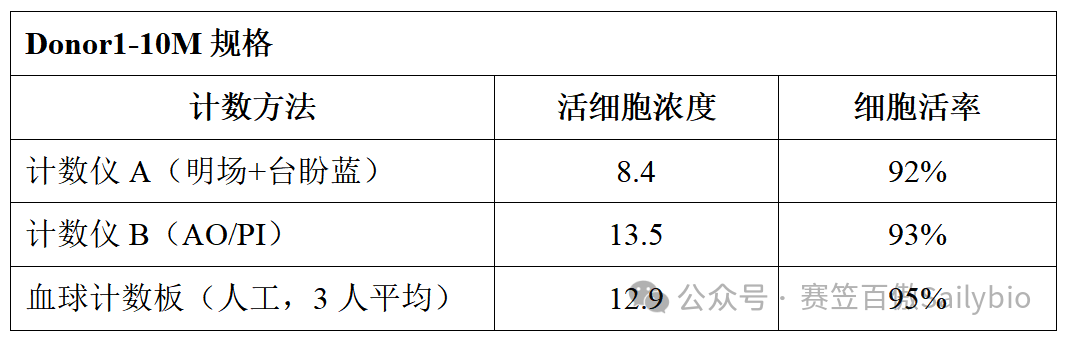
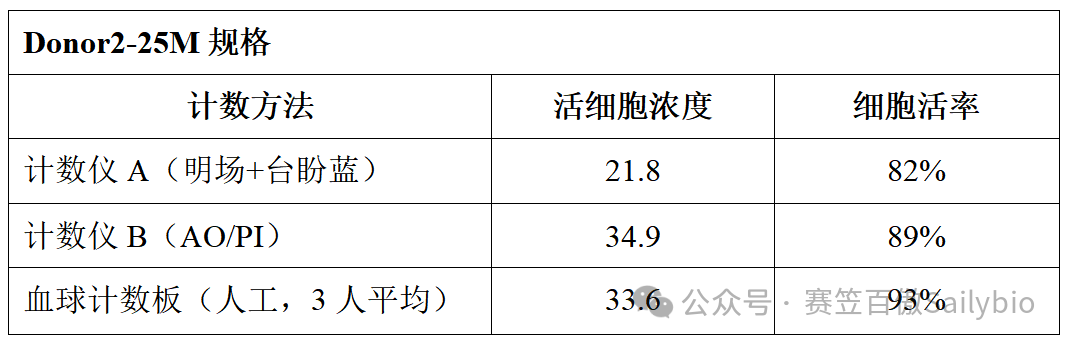
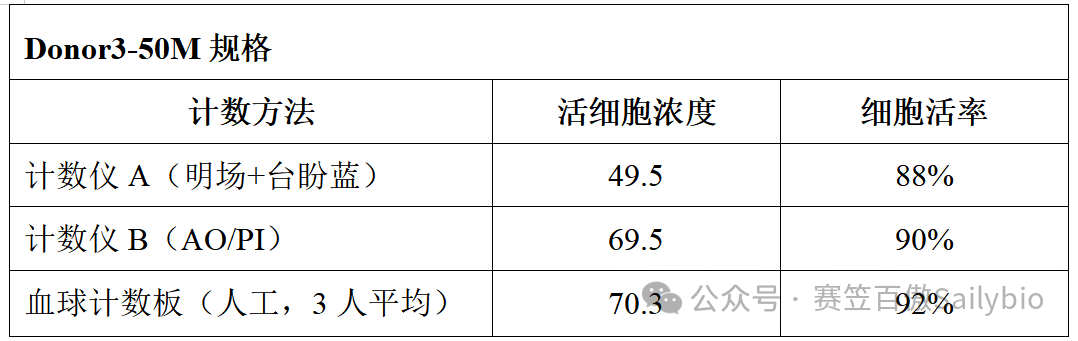
▶ 不同计数仪之间的活细胞浓度差异可达 20% 以上,活率差异在5%左右,有些计数仪会高估,有些会低估,如果你用高估的结果去做实验铺板,后果可想而知。
为什么PBMC复苏后“测不准”?
-
细胞聚团
冻存复苏后,PBMC容易形成小团块。普通明场计数仪会把2-3个细胞粘在一起当成1个,导致计数偏低。
-
死细胞与碎片干扰
复苏过程难免有部分细胞死亡,产生细胞碎片。台盼蓝染色有时无法完美区分碎片和小活细胞。
-
不同亚群大小差异
PBMC中淋巴细胞、单核细胞大小不同。有些计数仪对非典型大小的细胞识别不准。
-
计数原理不同
⏩ 明场+台盼蓝:依赖染料排除法,容易受碎片和聚团影响,且受仪器参数影响很大。
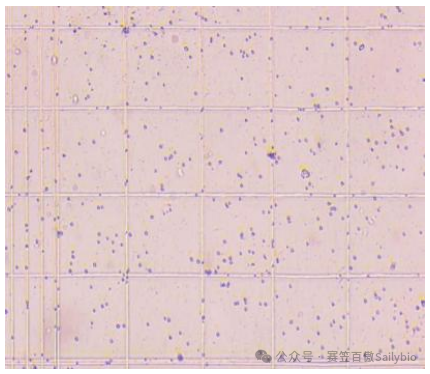
⏩ 人工血球计数板:依赖操作者经验,主观性强,但是更接近于真实细胞数量。
使用建议
✅ 1.同一实验周期内固定使用同一种计数仪
比“绝对准确”更重要的是一致性。前后对照实验,不要随意换计数仪。
✅ 2. 复苏后务必“静置休息”再计数
PBMC复苏后,建议在完全培养基中37℃静置1~2小时,让细胞状态稳定。
✅ 3. 用荧光计数仪及参数校正
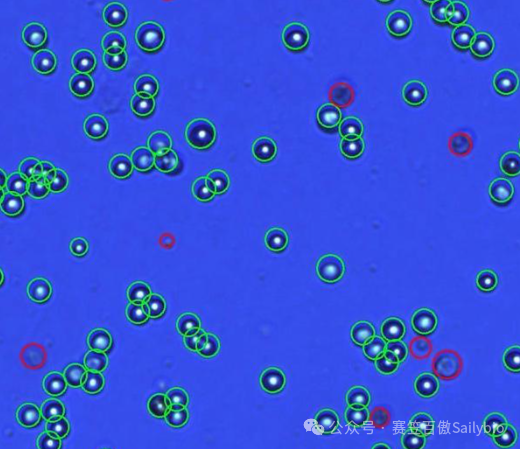
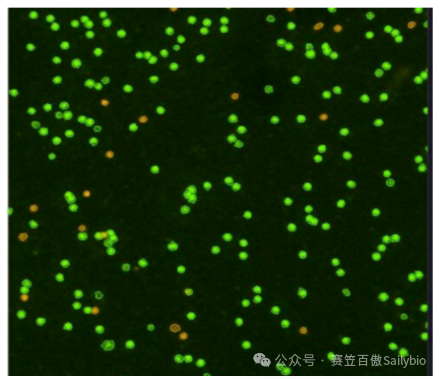
目前国际上公认最快速精准的PBMC计数方法是AO/PI双荧光染色法【1】。AO和PI都是细胞核染料,只有有核细胞会被染色,无核细胞,细胞碎片及其他杂质不发光;这样就排除了红细胞、血小板等干扰因素。同时活细胞会被AO染色为绿色荧光,死细胞会被PI染色为红色荧光,在精准计数的同时也获得了精准的细胞活率。

✅ 4.仪器校准
因PBMC细胞群体的复杂性,在使用细胞计数仪计数时,需要对细胞计数仪的参数进行定制化调整,以获得准确的计数结果;细胞计数时需要将细胞密度调整至仪器计数合适的密度范围,过高或过低都易导致细胞计数结果不准。
温馨小提示
➡ 不同计数仪之间的差异有可能是“仪器误差”,也可能是系统性偏差。作为科研或生产人员,我们要做的不是盲目相信屏幕上的数字,而是:
理解方法差异 → 固定操作标准 → 交叉验证精度
【1】Chan L L Y, Laverty D J, Smith T, et al. Accurate measurement of peripheral blood mononuclear cell concentration using image cytometry to eliminate RBC-induced counting error[J]. Journal of immunological methods, 2013, 388(1-2): 25-32.
.png)
.jpg)